–Т —Б—В–∞—В—М–µ —З–Є—В–∞—В–µ–ї—М —Г–Ј–љ–∞–µ—В –њ–Њ–і—А–Њ–±–љ–Њ—Б—В–Є –≤–љ—Г—В—А–µ–љ–љ–µ–є –ґ–Є–Ј–љ–Є –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –Є–Ј—Г—З–µ–љ–Є—П –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –њ—А–Њ–Ї–∞—А–Є–Њ—В –¶–µ–љ—В—А–∞ –љ–∞—Г–Ї –Њ –ґ–Є–Ј–љ–Є –≤ –°–Ї–Њ–ї–Ї–Њ–≤—Б–Ї–Њ–Љ –Є–љ—Б—В–Є—В—Г—В–µ –љ–∞—Г–Ї–Є –Є —В–µ—Е–љ–Њ–ї–Њ–≥–Є–є –Є –µ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М—Б–Ї–Њ–є —А–∞–±–Њ—В—Л
–Э–∞–і–Њ —В–Њ–ї—М–Ї–Њ –ї—О–±–Є—В—М —В–Њ, —З—В–Њ —В—Л –і–µ–ї–∞–µ—И—М, –Є –Њ—З–µ–љ—М –Љ–љ–Њ–≥–Њ —А–∞–±–Њ—В–∞—В—М.
–Ъ–Њ–љ—Б—В–∞–љ—В–Є–љ –°–µ–≤–µ—А–Є–љ–Њ–≤
–°—В—Г–і–µ–љ—В—Л, —Г–ґ–µ –њ–Њ–ї—Г—З–Є–≤—И–Є–µ —Б—В–µ–њ–µ–љ—М –Љ–∞–≥–Є—Б—В—А–∞, —А–∞—Б—Б–Ї–∞–Ј—Л–≤–∞—О—В –Њ –њ–ї–∞–љ–Є—А—Г–µ–Љ—Л—Е —В–µ–Љ–∞—Е –Ї–∞–љ–і–Є–і–∞—В—Б–Ї–Є—Е –і–Є—Б—Б–µ—А—В–∞—Ж–Є–є, —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е: ¬Ђ–•–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ —В–µ–ї–Њ–Љ–µ—А–∞–Ј—Л –≤ —Б–µ–Љ–µ–є—Б—В–≤–µ –Ї—А–µ—Б—В–Њ—Ж–≤–µ—В–љ—Л—Е¬ї, ¬Ђ–Т–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ Clostridium difficile –Є –±–∞–Ї—В–µ—А–Є–Њ—Д–∞–≥–∞ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Д–∞–≥–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є¬ї –Є ¬Ђ–Ю—Д—Д—В–∞—А–≥–µ—В–љ–∞—П –і–µ–≥—А–∞–і–∞—Ж–Є—П –Ї–ї–µ—В–Њ—З–љ—Л—Е –†–Э–Ъ, –≤—Л–Ј–≤–∞–љ–љ–∞—П –љ—Г–Ї–ї–µ–∞–Ј–Њ–є CRISPR-Cas13a¬ї.
–†—Г–Ї–Њ–≤–Њ–і–Є—В–µ–ї—М –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –≤ –і–Њ–≤–Њ–ї—М–љ–Њ –љ–µ–њ—А–Є–љ—Г–ґ–і–µ–љ–љ–Њ–є –Љ–∞–љ–µ—А–µ –Ї—А–Є—В–Є–Ї—Г–µ—В —А–∞–±–Њ—В—Л —Б—В—Г–і–µ–љ—В–Њ–≤, –±–µ–≥–ї–Њ –≤—Л—П–≤–ї—П—П —Б–ї–∞–±—Л–µ –Љ–µ—Б—В–∞ –Є –≤–љ–Њ—Б—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–µ –њ—А–∞–≤–Ї–Є. –°—А–∞–Ј—Г –±—А–Њ—Б–∞–µ—В—Б—П –≤ –≥–ї–∞–Ј–∞ —А–∞—Б—Б–ї–∞–±–ї–µ–љ–љ–∞—П –∞—В–Љ–Њ—Б—Д–µ—А–∞, —Б–Њ–≤—Б–µ–Љ –љ–µ –њ–Њ—Е–Њ–ґ–∞—П –љ–∞ –њ—А–µ–і–Ј–∞—Й–Є—В—Л –Є –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ —Б–Њ–±—А–∞–љ–Є—П –≤ —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В–µ. –Ґ–∞–Ї–Њ–є –љ–µ–Њ–±—Л—З–љ—Л–є –і–ї—П –≤—Г–Ј–∞ –Є ¬Ђ–Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Њ–є –∞–Ї–∞–і–µ–Љ–Є–Є¬ї —Б—В–Є–ї—М –љ–∞–њ–Њ–Љ–Є–љ–∞–µ—В —Б–Ї–Њ—А–µ–µ —А–∞–±–Њ—В—Г –Ї–Њ–Љ–∞–љ–і—Л –і–Њ–Ї—В–Њ—А–∞ –•–∞—Г—Б–∞.
–І—В–Њ –ґ–µ —Н—В–Њ? –≠—В–Њ lab meeting –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М—Б–Ї–Њ–є –≥—А—Г–њ–њ—Л –Ъ–Њ–љ—Б—В–∞–љ—В–Є–љ–∞ –°–µ–≤–µ—А–Є–љ–Њ–≤–∞ –Є–Ј –¶–µ–љ—В—А–∞ –љ–∞—Г–Ї –Њ –ґ–Є–Ј–љ–Є (Center of Life Sciences, CLS) –°–Ї–Њ–ї—В–µ—Е–∞, –њ–Њ—Б–≤—П—Й–µ–љ–љ—Л–є –±—Г–і—Г—Й–Є–Љ –∞—Б–њ–Є—А–∞–љ—В—Б–Ї–Є–Љ —А–∞–±–Њ—В–∞–Љ.
 –Ъ–Њ–љ—Б—В–∞–љ—В–Є–љ –°–µ–≤–µ—А–Є–љ–Њ–≤ |
–Ш–љ–і–µ–Ї—Б –•–Є—А—И–∞: 63. –Э–∞—Г—З–љ—Л–µ –Є–љ—В–µ—А–µ—Б—Л–Ь–µ—В–∞–±–Њ–ї–Є–Ј–Љ –њ—А–Њ–Ї–∞—А–Є–Њ—В, –∞ –Є–Љ–µ–љ–љ–Њ –Є—Е –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П —Б –≤–Є—А—Г—Б–∞–Љ–Є –Є –і—А—Г–≥ —Б –і—А—Г–≥–Њ–Љ. –°—О–і–∞ –Њ—В–љ–Њ—Б—П—В—Б—П –Є –Є–Ј—Г—З–µ–љ–Є–µ –Љ–Є–Ї—А–Њ—Ж–Є–љ–Њ–≤ (—Н—В–Њ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є, –љ–∞—Ж–µ–ї–µ–љ–љ—Л–µ –љ–∞ –і—А—Г–≥–Є–µ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ—Л), –Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П CRISPR-—Б–Є—Б—В–µ–Љ, –Є –љ–∞—Г—З–љ—Л–µ –Є–Ј—Л—Б–Ї–∞–љ–Є—П –≤ –Њ–±–ї–∞—Б—В–Є –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є–Є –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –≥–µ–љ–Њ–Љ–∞. –Ю–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–°–µ–≤–µ—А–Є–љ–Њ–≤ –≤ 1990 –≥–Њ–і—Г –Њ–Ї–Њ–љ—З–Є–ї –±–Є–Њ—Д–∞–Ї –Ь–У–£, –Ј–∞—В–µ–Љ –љ–µ–Ї–Њ—В–Њ—А–Њ–µ –≤—А–µ–Љ—П —А–∞–±–Њ—В–∞–ї –≤ –Я—Г—Й–Є–љ–Њ. –Х—Й–µ –љ–∞ –њ—П—В–Њ–Љ –Ї—Г—А—Б–µ –њ—А–Њ—И–µ–ї —Б—В–∞–ґ–Є—А–Њ–≤–Ї—Г –≤ –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –С—А–Є—Б—В–Њ–ї—М—Б–Ї–Њ–≥–Њ —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В–∞ –≤ –Т–µ–ї–Є–Ї–Њ–±—А–Є—В–∞–љ–Є–Є. –Я–Њ—Б–ї–µ —Н—В–Њ–≥–Њ –њ–Њ—Б—В—Г–њ–Є–ї –≤ –∞—Б–њ–Є—А–∞–љ—В—Г—А—Г –Ш–љ—Б—В–Є—В—Г—В–∞ –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–є –≥–µ–љ–µ—В–Є–Ї–Є –†–Р–Э, –Њ—В–Ї—Г–і–∞ –њ–Њ –њ—А–Њ–≥—А–∞–Љ–Љ–µ –Њ–±–Љ–µ–љ–∞ –Љ–Њ–ї–Њ–і—Л–Љ–Є —Г—З–µ–љ—Л–Љ–Є –Ф–ґ–Њ—А–і–ґ–∞ –°–Њ—А–Њ—Б–∞ —Г–µ—Е–∞–ї –≤ –°–®–Р –Є –і–≤–∞ –≥–Њ–і–∞ —А–∞–±–Њ—В–∞–ї –≤ –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –Ъ–Њ–ї—Г–Љ–±–Є–є—Б–Ї–Њ–≥–Њ —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В–∞ —Г –Р–ї–Є–Ї–∞ –У–Њ–ї—М–і—Д–∞—А–±–∞. –Я–Њ—Б–ї–µ —Н—В–Њ–≥–Њ –≤–µ—А–љ—Г–ї—Б—П –≤ –†–Њ—Б—Б–Є—О –Є –≤ 1993 –≥–Њ–і—Г –Ј–∞—Й–Є—В–Є–ї –Ї–∞–љ–і–Є–і–∞—В—Б–Ї—Г—О –і–Є—Б—Б–µ—А—В–∞—Ж–Є—О –њ–Њ —В–µ–Љ–µ ¬Ђ–Ф–Њ–Љ–µ–љ–љ–∞—П –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є—П –±–µ—В–∞-—Б—Г–±—К–µ–і–Є–љ–Є—Ж—Л –†–Э–Ъ-–њ–Њ–ї–Є–Љ–µ—А–∞–Ј—Л Escherichia coli¬ї. –Ъ–∞—А—М–µ—А–∞–°–µ–≤–µ—А–Є–љ–Њ–≤ —А–∞–±–Њ—В–∞–ї –≤ –°–®–Р: —Б–љ–∞—З–∞–ї–∞ –≤ –†–Њ–Ї—Д–µ–ї–ї–µ—А–Њ–≤—Б–Ї–Њ–Љ —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В–µ, –њ–Њ–Ј–ґ–µ —Б—В–∞–ї –њ—А–Њ—Д–µ—Б—Б–Њ—А–Њ–Љ –Ш–љ—Б—В–Є—В—Г—В–∞ –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є–Є –Т–∞–Ї—Б–Љ–∞–љ–∞ –≤ –†–∞—В–≥–µ—А—Б–Ї–Њ–Љ —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В–µ, –≥–і–µ –≤–Њ–Ј–≥–ї–∞–≤–Є–ї —Б–≤–Њ—О –ї–∞–±–Њ—А–∞—В–Њ—А–Є—О, –∞–Ї—В–Є–≤–љ–Њ —А–∞–±–Њ—В–∞—О—Й—Г—О –і–Њ —Б–Є—Е –њ–Њ—А. –Т 2005 –≥–Њ–і—Г –Њ—А–≥–∞–љ–Є–Ј–Њ–≤–∞–ї —Б–Њ–±—Б—В–≤–µ–љ–љ—Г—О –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М—Б–Ї—Г—О –≥—А—Г–њ–њ—Г –≤ –Ш–љ—Б—В–Є—В—Г—В–µ –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–є –≥–µ–љ–µ—В–Є–Ї–Є –†–Р–Э. –Т 2011-–Љ –°–µ–≤–µ—А–Є–љ–Њ–≤ –≤—Е–Њ–і–Є–ї –≤ ¬Ђ–Ј–∞–њ—Г—Б–Ї–∞—О—Й—Г—О –Ї–Њ–Љ–∞–љ–і—Г¬ї —Б–Њ–Ј–і–∞–љ–Є—П –°–Ї–Њ–ї—В–µ—Е–∞. –Т 2013 –≥–Њ–і—Г –Ј–∞—П–≤–Ї–∞ –°–µ–≤–µ—А–Є–љ–Њ–≤–∞ –≤—Л–Є–≥—А–∞–ї–∞ –Ї–Њ–љ–Ї—Г—А—Б –Љ–µ–≥–∞–≥—А–∞–љ—В–Њ–≤, –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ –Њ–љ —А–µ—И–Є–ї –Њ—Б–љ–Њ–≤–∞—В—М –ї–∞–±–Њ—А–∞—В–Њ—А–Є—О –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–є –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є–Є –≤ –Я–Њ–ї–Є—В–µ—Е–љ–Є—З–µ—Б–Ї–Њ–Љ —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В–µ –°–∞–љ–Ї—В-–Я–µ—В–µ—А–±—Г—А–≥–∞. –°–µ–є—З–∞—Б –њ–Њ–Љ–Є–Љ–Њ –≥—А—Г–њ–њ—Л –≤ –°–Ї–Њ–ї—В–µ—Е–µ –Ъ–Њ–љ—Б—В–∞–љ—В–Є–љ –Т–Є–Ї—В–Њ—А–Њ–≤–Є—З –Ј–∞–≤–µ–і—Г–µ—В –ї–∞–±–Њ—А–∞—В–Њ—А–Є—П–Љ–Є —А–µ–≥—Г–ї—П—Ж–Є–Є —Н–Ї—Б–њ—А–µ—Б—Б–Є–Є –≥–µ–љ–Њ–≤ –Љ–Њ–±–Є–ї—М–љ—Л—Е —Н–ї–µ–Љ–µ–љ—В–Њ–≤ –њ—А–Њ–Ї–∞—А–Є–Њ—В –≤ –Ш–љ—Б—В–Є—В—Г—В–µ –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–є –≥–µ–љ–µ—В–Є–Ї–Є (–Ш–Ь–У) –†–Р–Э, –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–є –≥–µ–љ–µ—В–Є–Ї–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –≤ –Ш–љ—Б—В–Є—В—Г—В–µ –±–Є–Њ–ї–Њ–≥–Є–Є –≥–µ–љ–∞ (–Ш–С–У) –†–Р–Э, –љ–∞ –±–∞–Ј–µ –Ї–Њ—В–Њ—А–Њ–є —Б–Њ–Ј–і–∞–љ–∞ –Ї–∞—Д–µ–і—А–∞ –°–Ї–Њ–ї—В–µ—Е–∞, –∞ —В–∞–Ї–ґ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М—Б–Ї–Є–Љ —Ж–µ–љ—В—А–Њ–Љ –°–Ї–Њ–ї—В–µ—Е–∞ –≤ –°–Я–±–У–£ –Є –ї–∞–±–Њ—А–∞—В–Њ—А–Є–µ–є –≤ –†–∞—В–≥–µ—А—Б–Ї–Њ–Љ —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В–µ –≤ –°–®–Р. –Ґ–∞–Ї–ґ–µ, –њ–Њ –≤–µ—А—Б–Є—П–Љ Web of Science –Є Scopus, –°–µ–≤–µ—А–Є–љ–Њ–≤ —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј —Б–∞–Љ—Л—Е —Ж–Є—В–Є—А—Г–µ–Љ—Л—Е —Г—З–µ–љ—Л—Е –≤ –†–Њ—Б—Б–Є–Є. |
–Ъ–∞—А—М–µ—А–љ—Л–є –њ—Г—В—М –°–µ–≤–µ—А–Є–љ–Њ–≤–∞ –≤–µ—Б—М–Љ–∞ –Є–Ј–≤–Є–ї–Є—Б—В. –Т–Њ—В —В–∞–Ї —А–∞—Б—Б–Ї–∞–Ј—Л–≤–∞–µ—В –Њ –љ–µ–Љ –Р–љ–љ–∞ –Ы–Њ–њ–∞—В–Є–љ–∞, –±—Л–≤—И–∞—П –∞—Б–њ–Є—А–∞–љ—В–Ї–∞ –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –°–µ–≤–µ—А–Є–љ–Њ–≤–∞ –≤ –Ш–Ь–У, –Ї–Њ—В–Њ—А–∞—П —Б–µ–є—З–∞—Б —А–∞–±–Њ—В–∞–µ—В –њ–Њ—Б—В–і–Њ–Ї–Њ–Љ –≤ –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –†–Њ—В–µ–Љ–∞ –°–Њ—А–µ–Ї–∞ –≤ –Ш–љ—Б—В–Є—В—Г—В–µ –Т–µ–є—Ж–Љ–∞–љ–∞ –≤ –Ш–Ј—А–∞–Є–ї–µ:
"–ѓ –±—Л–ї–∞ —Б—В—Г–і–µ–љ—В–Ї–Њ–є –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є–Є –њ–Њ—З–≤ –Є –і–µ–ї–∞–ї–∞ –і–Є–њ–ї–Њ–Љ –њ–Њ –њ–Њ—З–≤–µ–љ–љ—Л–Љ –±–∞–Ї—В–µ—А–Є–Њ—Д–∞–≥–∞–Љ. –Ъ –њ—П—В–Њ–Љ—Г –Ї—Г—А—Б—Г —Б—В–∞–ї–Њ –њ–Њ–љ—П—В–љ–Њ (–Є–Ј —Б—В–∞—В–µ–є –Є –њ–Њ —Б–ї—Г—Е–∞–Љ), —З—В–Њ –Ъ–Њ–љ—Б—В–∞–љ—В–Є–љ вАФ —Б–∞–Љ—Л–є —Б–Є–ї—М–љ—Л–є —Г—З–µ–љ—Л–є –≤ —Б—В—А–∞–љ–µ, —Г –Ї–Њ—В–Њ—А–Њ–≥–Њ –Љ–Њ–ґ–љ–Њ –±—Л–ї–Њ –±—Л –њ—А–Њ–і–Њ–ї–ґ–Є—В—М –Є–Ј—Г—З–∞—В—М —Д–∞–≥–Њ–≤. –ѓ –µ–Љ—Г –љ–∞–њ–Є—Б–∞–ї–∞, –Є –Њ–љ –≤–Ј—П–ї –Љ–µ–љ—П –≤ –∞—Б–њ–Є—А–∞–љ—В—Г—А—Г –≤ –Ш–Ь–У. –≠—В–Њ –±—Л–ї 2008 –≥–Њ–і, –Њ–љ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ –љ–µ–і–∞–≤–љ–Њ –≤–µ—А–љ—Г–ї—Б—П –≤ –†–Њ—Б—Б–Є—О. –Я–µ—А–≤—Л–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –ї–µ—В –∞—Б–њ–Є—А–∞–љ—В—Г—А—Л —П –Ј–∞–љ–Є–Љ–∞–ї–∞—Б—М –Љ–Є–Ї—А–Њ–±–љ—Л–Љ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–Є–µ–Љ —Б–љ–µ–≥–∞ –Р–љ—В–∞—А–Ї—В–Є–Ї–Є –Є –µ–Ј–і–Є–ї–∞ —В—Г–і–∞ –і–≤–∞ —А–∞–Ј–∞ –≤ —Н–Ї—Б–њ–µ–і–Є—Ж–Є—О, –∞ –њ–Њ—В–Њ–Љ —Г–ґ–µ –њ–µ—А–µ–Ї–ї—О—З–Є–ї–∞—Б—М –љ–∞ —В–µ—А–Љ–∞–ї—М–љ—Л–µ –Є—Б—В–Њ—З–љ–Є–Ї–Є —Б –Є—Е —Д–∞–≥–∞–Љ–Є –Є –Ї—А–Є—Б–њ—А–∞–Љ–Є (—П –±—Л–ї–∞ –≤ —З–Є—Б–ї–µ —В–µ—Е, –Ї—В–Њ –њ–Њ–ї–Њ–ґ–Є–ї –љ–∞—З–∞–ї–Њ –Є–Ј—Г—З–µ–љ–Є—О –≤—Б–µ—Е —Н—В–Є—Е –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–є –≤ –ї–∞–±–µ). –Т —В–Њ –≤—А–µ–Љ—П –±—Л–ї–Є –µ—Й–µ –љ–∞ –њ–Њ–і—К–µ–Љ–µ —В–µ–Љ—Л –Љ–Є–Ї—А–Њ—Ж–Є–љ–Њ–≤, –њ–Њ–ї–Є–Љ–µ—А–∞–Ј—Л –±–∞–Ї—В–µ—А–Є–Њ—Д–∞–≥–Њ–≤ –Є –і–∞–ґ–µ —Г–ґ–µ –љ–∞—З–Є–љ–∞–ї–Є—Б—М –Ї—А–Є—Б–њ—А—Л. –°–Њ –≤—А–µ–Љ–µ–љ–µ–Љ —Б—В–∞–ї–Њ –≤—Б—С –±–Њ–ї—М—И–µ –Ј–∞—Й–Є—В–љ—Л—Е —Б–Є—Б—В–µ–Љ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ —В–Є–њ–∞ –Ї—А–Є—Б–њ—А–Њ–≤ –Є BREX (–Њ–± —Н—В–Њ–Љ —З–Є—В–∞–є—В–µ –љ–Є–ґ–µ вАФ –њ—А–Є–Љ. –∞–≤—В–Њ—А–∞). –Т 2015вАУ2016 –≥–Њ–і–∞—Е –њ–Њ–ї–Њ–≤–Є–љ–∞ –∞—Б–њ–Є—А–∞–љ—В–Њ–≤ —В–Њ–є –њ–µ—А–≤–Њ–є –≤–Њ–ї–љ—Л —А–∞–Ј—К–µ—Е–∞–ї–∞—Б—М, –Є –≤ –ї–∞–±–µ –њ–Њ—П–≤–Є–ї–Њ—Б—М –Њ–≥—А–Њ–Љ–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Г–ґ–µ —Б–Ї–Њ–ї—В–µ—Е–Њ–≤—Б–Ї–Є—Е —Б—В—Г–і–µ–љ—В–Њ–≤".

CRISPR? –Р–љ—В–Є–±–Є–Њ—В–Є–Ї–Є? –Т—Б—С –≤–Љ–µ—Б—В–µ!
–Ю—Б–љ–Њ–≤–љ—Л–µ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –Ъ–Њ–љ—Б—В–∞–љ—В–Є–љ–∞ –°–µ–≤–µ—А–Є–љ–Њ–≤–∞ –≤ –°–Ї–Њ–ї—В–µ—Е–µ вАФ –Љ–љ–Њ–≥–Њ–Њ–±—А–∞–Ј–Є–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–є –±–∞–Ї—В–µ—А–Є–є –Є –≤–Є—А—Г—Б–Њ–≤, –∞ —В–∞–Ї–ґ–µ –њ–Њ–Є—Б–Ї –љ–Њ–≤—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤. –Ю–±—К–µ–і–Є–љ—П–µ—В –Њ–±–µ —В–µ–Љ—Л –Њ–і–љ–Њ вАФ —Н—В–Њ —Б–њ–Њ—Б–Њ–±—Л –±–∞–Ї—В–µ—А–Є–є –Ј–∞—Й–Є—Й–∞—В—М—Б—П –Є –∞—В–∞–Ї–Њ–≤–∞—В—М.–Т–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ –≤–Є—А—Г—Б–Њ–≤ –Є –±–∞–Ї—В–µ—А–Є–є–Ю–і–љ–∞ –Є–Ј –њ–µ—А–µ–і–Њ–≤—Л—Е —В–µ–Љ –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–є –±–Є–Њ–ї–Њ–≥–Є–Є вАФ –Ј–∞–≤–Њ–µ–≤–∞–≤—И–Є–µ –љ–µ–≤–µ—А–Њ—П—В–љ—Г—О —Б–ї–∞–≤—Г –і–∞–ґ–µ –Ј–∞ –њ—А–µ–і–µ–ї–∞–Љ–Є –љ–∞—Г—З–љ—Л—Е –Ї—А—Г–≥–Њ–≤ CRISPR/Cas-—Б–Є—Б—В–µ–Љ—Л [4]. –Ь–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ–Є –Є—Е —А–∞–±–Њ—В—Л —Б –њ–Њ–Ј–Є—Ж–Є–є —Н–≤–Њ–ї—О—Ж–Є–Є –Є —Н–Ї–Њ–ї–Њ–≥–Є–Є вАФ —В–Њ –µ—Б—В—М –Є–Ј—Г—З–µ–љ–Є–µ–Љ –њ—А–Є–љ—Ж–Є–њ–Њ–≤ —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—П –Є –≤–ї–Є—П–љ–Є—П CRISPR –љ–∞ –Љ–Є–Ї—А–Њ–±–љ—Л–µ —Б–Њ–Њ–±—Й–µ—Б—В–≤–∞ (–∞ –љ–µ —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞–љ–Є–µ–Љ –≥–µ–љ–Њ–Љ–Њ–≤, –Ї–∞–Ї –Љ–Њ–ґ–љ–Њ –±—Л–ї–Њ –±—Л –њ–Њ–і—Г–Љ–∞—В—М), вАФ –Ј–∞–љ–Є–Љ–∞–µ—В—Б—П –Є –ї–∞–±–Њ—А–∞—В–Њ—А–Є—П –°–µ–≤–µ—А–Є–љ–Њ–≤–∞.–Э–∞ –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ—Л–є –≤–Њ–њ—А–Њ—Б –Њ–± –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є CRISPR-—Б–Є—Б—В–µ–Љ –≤ –±–Є–Њ—В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є, –Ї–Њ—В–Њ—А—Л–є —В–∞–Ї —З–∞—Б—В–Њ –Ј–≤—Г—З–Є—В –≤ –њ—Г–±–ї–Є—З–љ—Л—Е –Њ–±—Б—Г–ґ–і–µ–љ–Є—П—Е, —А—Г–Ї–Њ–≤–Њ–і–Є—В–µ–ї—М –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –Њ—В–≤–µ—З–∞–µ—В –±–µ–Ј —Н–љ—В—Г–Ј–Є–∞–Ј–Љ–∞. ¬Ђ–Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ [CRISPR-—Б–Є—Б—В–µ–Љ] –≤ –±–Є–Њ—В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є –љ–∞—Б—В–Њ–ї—М–Ї–Њ —Б–Ї—Г—З–љ–Њ –Є –љ–µ–Є–љ—В–µ—А–µ—Б–љ–Њ, —З—В–Њ...¬ї вАФ —Г–і—А—Г—З–µ–љ–љ–Њ –Ї–∞—З–∞–µ—В –≥–Њ–ї–Њ–≤–Њ–є –°–µ–≤–µ—А–Є–љ–Њ–≤ –Є —В—Г—В –ґ–µ –њ—А–Є–≤–Њ–і–Є—В –≤ –њ—А–Є–Љ–µ—А —А–µ—Б—В—А–Є–Ї—В–∞–Ј—Л, –Ї–Њ—В–Њ—А—Л–µ —Б–Њ—А–Њ–Ї –ї–µ—В –љ–∞–Ј–∞–і –њ—А–Њ–Є–Ј–≤–µ–ї–Є –±—Г–Љ, –Ї–∞–Ї —Б–µ–≥–Њ–і–љ—П CRISPR/Cas, –Њ–і–љ–∞–Ї–Њ —В–µ–њ–µ—А—М –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В –Є–љ—В–µ—А–µ—Б –ї–Є—И—М –Ї–∞–Ї –Є–љ—Б—В—А—Г–Љ–µ–љ—В –≥–µ–љ–љ–Њ–є –Є–љ–ґ–µ–љ–µ—А–Є–Є.

–Ъ—А–Є—Б–њ—А—Л вАФ —Н—В–Њ –љ–µ —В–Њ–ї—М–Ї–Њ —Ж–µ–љ–љ—Л–є –Љ–µ—Е –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л–є –Є–љ—Б—В—А—Г–Љ–µ–љ—В —А–µ–і–∞–Ї—В–Є—А–Њ–≤–∞–љ–Є—П –≥–µ–љ–Њ–Љ–∞, –љ–Њ –µ—Й–µ –Є ¬Ђ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–∞—П –ї–µ—В–Њ–њ–Є—Б—М¬ї –Ї–∞–ґ–і–Њ–≥–Њ —И—В–∞–Љ–Љ–∞ –±–∞–Ї—В–µ—А–Є–є. –°–њ–µ–є—Б–µ—А—Л –≤ CRISPR-–Ї–∞—Б—Б–µ—В–µ (—Д—А–∞–≥–Љ–µ–љ—В—Л –≥–µ–љ–Њ–Љ–Њ–≤ —Д–∞–≥–Њ–≤ –Є –њ–ї–∞–Ј–Љ–Є–і, –њ–Њ–Љ–µ—Й–µ–љ–љ—Л–µ –≤ ¬Ђ–≥–µ–љ–Њ–Љ–љ—Г—О –±–Є–±–ї–Є–Њ—В–µ–Ї—Г¬ї —Е–Њ–Ј—П–Є–љ–∞) –њ–Њ–Ј–≤–Њ–ї—П—О—В —Б—Г–і–Є—В—М –Њ ¬Ђ–њ—А–Њ—И–ї–Њ–Љ¬ї –±–∞–Ї—В–µ—А–Є–Є.
–Т–Њ–Њ–±—Й–µ, CRISPR/Cas –≤ –њ—А–Є—А–Њ–і–µ вАФ –Њ—В–љ—О–і—М –љ–µ ¬Ђ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –љ–Њ–ґ–љ–Є—Ж—Л¬ї –љ–∞ –њ–Њ—В–µ—Е—Г –±–Є–Њ—В–µ—Е–љ–Њ–ї–Њ–≥–∞–Љ, –∞ —Б–Є—Б—В–µ–Љ–∞ –∞–і–∞–њ—В–Є–≤–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ –њ—А–Њ–Ї–∞—А–Є–Њ—В, –Ї–Њ—В–Њ—А–∞—П ¬Ђ–Ј–∞–њ–Њ–Љ–Є–љ–∞–µ—В¬ї –∞–≥—А–µ—Б—Б–Њ—А–∞ (–≤–Є—А—Г—Б –Є–ї–Є —З—Г–ґ–µ—А–Њ–і–љ—Г—О –њ–ї–∞–Ј–Љ–Є–і—Г) –њ—Г—В–µ–Љ –≤–љ–µ—Б–µ–љ–Є—П —З–∞—Б—В–µ–є –≥–µ–љ–Њ–Љ–∞ ¬Ђ–њ—А–Є—И–µ–ї—М—Ж–∞¬ї –≤ —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л–є –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–є –ї–Њ–Ї—Г—Б —Е–Њ–Ј—П–Є–љ–∞ вАФ –≤ —В—Г —Б–∞–Љ—Г—О ¬Ђ–Ї–∞—Б—Б–µ—В—Г¬ї. –Я—А–Є —Б–ї–µ–і—Г—О—Й–µ–Љ –Ї–Њ–љ—В–∞–Ї—В–µ –±–∞–Ї—В–µ—А–Є—П, –љ–µ—Б—Г—Й–∞—П —Н—В–Є —Д—А–∞–≥–Љ–µ–љ—В—Л (—Б–њ–µ–є—Б–µ—А—Л) –≤ –≥–µ–љ–Њ–Љ–µ, —Б–њ–Њ—Б–Њ–±–љ–∞ –њ—А–Є—Ж–µ–ї—М–љ–Њ –≤–љ–µ—Б—В–Є —А–∞–Ј—А—Л–≤ –≤ –Ф–Э–Ъ —Д–∞–≥–∞/–њ–ї–∞–Ј–Љ–Є–і—Л, –∞ –Ј–љ–∞—З–Є—В вАФ –љ–µ–є—В—А–∞–ї–Є–Ј–Њ–≤–∞—В—М –∞–≥—А–µ—Б—Б–Њ—А–∞.
¬Ђ–Э–∞–±–Њ—А CRISPR-—Б–њ–µ–є—Б–µ—А–Њ–≤, –љ–∞—Е–Њ–і—П—Й–Є–є—Б—П –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є –±–∞–Ї—В–µ—А–Є–є, –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤–∞–Љ —Б—Г–і–Є—В—М –Њ –њ—А–Њ—И–ї—Л—Е –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П—Е –±–∞–Ї—В–µ—А–Є–є —Б –≤–Є—А—Г—Б–Њ–Љ. –°—А–∞–≤–љ–Є–≤–∞—П —В–∞–Ї–Є–µ –љ–∞–±–Њ—А—Л –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–Њ–њ—Г–ї—П—Ж–Є—П—Е –Њ–і–љ–Њ–≥–Њ –≤–Є–і–∞, –∞–љ–∞–ї–Є–Ј–Є—А—Г—П —Б–Њ—Б—В–∞–≤ —Б–њ–µ–є—Б–µ—А–Њ–≤ –Є –і–Є–љ–∞–Љ–Є–Ї—Г –µ–≥–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Љ–Њ–ґ–љ–Њ –Њ—Ж–µ–љ–Є—В—М –Є—Б—В–Њ—А–Є—О —Н—В–Є—Е –њ–Њ–њ—Г–ї—П—Ж–Є–є¬ї, вАФ –≥–Њ–≤–Њ—А–Є—В –°–µ–≤–µ—А–Є–љ–Њ–≤ –≤ –Є–љ—В–µ—А–≤—М—О ¬Ђ–С–Є–Њ–Љ–Њ–ї–µ–Ї—Г–ї–µ¬ї.
–°–Є—Б—В–µ–Љ—Л —А–µ—Б—В—А–Є–Ї—Ж–Є–Є-–Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–Є –Є–Ј—Г—З–∞—О—В –≤ –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –љ–µ –Ї–∞–Ї –Љ–µ—Е–∞–љ–Є–Ј–Љ –Ј–∞—Й–Є—В—Л –±–∞–Ї—В–µ—А–Є–є –Њ—В –≤–Є—А—Г—Б–Њ–≤, –∞ —Б –њ–Њ–Ј–Є—Ж–Є–є ¬Ђ—И—В—Г—А–Љ–∞¬ї –≤–Є—А—Г—Б–Њ–Љ —Н—В–Њ–≥–Њ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ ¬Ђ–±–∞—Б—В–Є–Њ–љ–∞¬ї. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є—Б—Б–ї–µ–і—Г—О—В —А–∞–±–Њ—В—Г —Б–Є—Б—В–µ–Љ—Л –Ј–∞—Й–Є—В—Л-—Б–∞–є–ї–µ–љ—Б–Є–љ–≥–∞.
–Я–Њ—З–µ–Љ—Г –ґ–µ –Њ–і–љ–Њ–є –Є–Ј —Ж–µ–љ—В—А–∞–ї—М–љ—Л—Е —В–µ–Љ –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –≤—Л–±—А–∞–ї–Є –Є–Љ–µ–љ–љ–Њ –Ї—А–Є—Б–њ—А—Л?
¬Ђ–° —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–Є—П, —Н—В–Њ –љ–∞–Є–±–Њ–ї–µ–µ –Є–љ—В–µ—А–µ—Б–љ–∞—П –і–ї—П –Є–Ј—Г—З–µ–љ–Є—П —В–µ–Љ–∞. –Т–Њ—В –≤—Л —Б–Љ–Њ—В—А–Є—В–µ –љ–∞ housekeeping-–≥–µ–љ—Л (–≥–µ–љ—Л –і–Њ–Љ–∞—И–љ–µ–≥–Њ —Е–Њ–Ј—П–є—Б—В–≤–∞, —В–Њ –µ—Б—В—М –Ф–Э–Ъ- –Є –†–Э–Ъ-–њ–Њ–ї–Є–Љ–µ—А–∞–Ј—Л, —А–†–Э–Ъ –Є –њ—А–Њ—З–Є–µ) вАФ –Њ–љ–Є –≤—Б–µ–≥–і–∞ –Њ–і–Є–љ–∞–Ї–Њ–≤—Л–µ –Є —Б–Ї—Г—З–љ—Л–µ. –Р –≤–Њ—В —Б–Є—Б—В–µ–Љ—Л –Ј–∞—Й–Є—В—Л –њ–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—О –Њ—З–µ–љ—М –±—Л—Б—В—А–Њ –Є–Ј–Љ–µ–љ—П—О—В—Б—П –Ј–∞ —Б—З–µ—В ¬Ђ–≥–Њ–љ–Ї–Є¬ї –Љ–µ–ґ–і—Г –≤–Є—А—Г—Б–Њ–Љ –Є –±–∞–Ї—В–µ—А–Є–µ–є, –Є–ї–Є –≤ –Њ–±—Й–µ–Љ —Б–ї—Г—З–∞–µ –Љ–µ–ґ–і—Г –∞—В–∞–Ї—Г—О—Й–Є–Љ –Є –Ј–∞—Й–Є—Й–∞—О—Й–Є–Љ—Б—П. –Ь–µ—Е–∞–љ–Є–Ј–Љ—Л —Н—В–Њ–≥–Њ –љ–µ–Њ–±—Л—З–∞–є–љ–Њ –Є–љ—В–µ—А–µ—Б–љ—Л¬ї, вАФ –Њ—В–≤–µ—З–∞–µ—В –Ъ–Њ–љ—Б—В–∞–љ—В–Є–љ –°–µ–≤–µ—А–Є–љ–Њ–≤. –Т —Б–ї—Г—З–∞–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–є –±–∞–Ї—В–µ—А–Є–є —Б –≤–Є—А—Г—Б–Њ–Љ вАФ —Н—В–Њ CRISPR, –≤ —Б–ї—Г—З–∞–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П –±–∞–Ї—В–µ—А–Є–є –і—А—Г–≥ —Б –і—А—Г–≥–Њ–Љ вАФ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є.
–Т 2018 –≥–Њ–і—Г –≤ —И–Є—А–Њ–Ї–Њ –Є–Ј–≤–µ—Б—В–љ–Њ–Љ –ґ—Г—А–љ–∞–ї–µ Proceedings of National Academy of Sciences of USA –≤—Л—И–ї–∞ –≤–∞–ґ–љ–∞—П —Б—В–∞—В—М—П –њ–Њ —Н—В–Њ–є —В–µ–Љ–µ: ¬Ђ–Я—А–µ–і—Б–Ї–∞–Ј–∞–љ–Є–µ –≥–µ–љ–Њ–≤, —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б CRISPR-Cas-—Б–Є—Б—В–µ–Љ–∞–Љ–Є, –њ–Њ –∞–љ–∞–ї–Є–Ј—Г —Б–Њ—Б–µ–і–љ–Є—Е –≥–µ–љ–Њ–≤¬ї [9]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ–Њ–Љ–Є–Љ–Њ –°–µ–≤–µ—А–Є–љ–Њ–≤–∞ —Г—З–∞—Б—В–≤–Њ–≤–∞–ї –µ–≥–Њ –∞—Б–њ–Є—А–∞–љ—В –°–µ—А–≥–µ–є –®–Љ–∞–Ї–Њ–≤ (–Ї–Њ—В–Њ—А—Л–є, –Ї—Б—В–∞—В–Є, –±—Л–ї –љ–∞–≥—А–∞–ґ–і–µ–љ –њ—А–µ–Љ–Є–µ–є –і–Є—А–µ–Ї—В–Њ—А–∞ –Э–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –Є–љ—Б—В–Є—В—Г—В–Њ–≤ –Ј–і–Њ—А–Њ–≤—М—П –°–®–Р –Ј–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ –Њ–±–ї–∞—Б—В–Є –љ–Њ–≤—Л—Е CRISPR-Cas-—Б–Є—Б—В–µ–Љ), –∞ —В–∞–Ї–ґ–µ –Є–Ј–≤–µ—Б—В–љ—Л–є –±–Є–Њ–Є–љ—Д–Њ—А–Љ–∞—В–Є–Ї –Є —Н–≤–Њ–ї—О—Ж–Є–Њ–љ–Є—Б—В –Х–≤–≥–µ–љ–Є–µ–є –Ъ—Г–љ–Є–љ. –Т –њ—Г–±–ї–Є–Ї–∞—Ж–Є–Є –Њ–њ–Є—Б–∞–љ–∞ –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–∞—П —Б—В—А–∞—В–µ–≥–Є—П –Є–і–µ–љ—В–Є—Д–Є–Ї–∞—Ж–Є–Є –Є –Њ—Ж–µ–љ–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є –±–µ–ї–Ї–Њ–≤, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б CRISPR-Cas-—Б–Є—Б—В–µ–Љ–∞–Љ–Є. –Ш—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є –≤–≤–µ–ї–Є —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М вАФ CRISPRicity (–і–Њ—Б–ї–Њ–≤–љ–Њ вАФ ¬ЂCRISPR–Є—З–љ–Њ—Б—В—М¬ї), –Њ–њ—А–µ–і–µ–ї—П—О—Й–Є–є ¬Ђ—Б–Є–ї—Г¬ї —Б–≤—П–Ј–Є CRISPR —Б –±–µ–ї–Њ–Ї-–Ї–Њ–і–Є—А—Г—О—Й–Є–Љ–Є –≥–µ–љ–∞–Љ–Є –∞—А—Е–µ–є –Є –±–∞–Ї—В–µ—А–Є–є –Є–Ј —Б–µ–Ї–≤–µ–љ–Є—А–Њ–≤–∞–љ–љ—Л—Е –≥–µ–љ–Њ–Љ–Њ–≤ –Є –њ—А–µ–і—Б—В–∞–≤–ї—П—О—Й–Є–є —Б–Њ–±–Њ–є –Њ—В–љ–Њ—И–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –≥–µ–љ–∞ –≤ —Б–≤—П–Ј–Ї–µ —Б CRISPR –Ї –Њ–±—Й–µ–є —З–∞—Б—В–Њ—В–µ –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –≥–µ–љ–∞. –У–µ–љ—Л —Б —Н—В–Є–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –∞–љ–∞–ї–Њ–≥–Є—З–љ–Њ –°as-–≥–µ–љ–∞–Љ, —А–∞–љ–µ–µ –љ–µ –Њ—В–љ–Њ—Б—П—Й–Є–Љ—Б—П –Ї —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—О CRISPR-Cas —Б–Є—Б—В–µ–Љ—Л, –∞ –Ї–Њ–і–Є—А—Г–µ–Љ—Л–µ –Є–Љ–Є –±–µ–ї–Ї–Є –њ—А–Њ–≤–µ—А—П–ї–Є –∞–љ–∞–ї–Є–Ј–Њ–Љ –і–Њ–Љ–µ–љ–љ–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л –Є –Ї–Њ—Н–≤–Њ–ї—О—Ж–Є–Њ–љ–љ—Л–Љ –∞–љ–∞–ї–Є–Ј–Њ–Љ. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –±—Л–ї–Њ –љ–∞–є–і–µ–љ–Њ 79 –љ–Њ–≤—Л—Е –±–µ–ї–Њ–Ї-–Ї–Њ–і–Є—А—Г—О—Й–Є—Е –≥–µ–љ–Њ–≤, –≤–Њ–≤–ї–µ—З–µ–љ–љ—Л—Е –≤ —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є–µ CRISPR-Cas .
–Ъ–∞–Ї –ґ–µ —Б—В–∞–ї–Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –њ—А–µ–і—Б–Ї–∞–Ј—Л–≤–∞—В—М –љ–Њ–≤—Л–µ –≥–µ–љ—Л –≤ —Б–Є—Б—В–µ–Љ–µ –∞–і–∞–њ—В–Є–≤–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ –њ—А–Њ–Ї–∞—А–Є–Њ—В? –£ –±–∞–Ї—В–µ—А–Є–є –Є –∞—А—Е–µ–є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ —Б–≤—П–Ј–∞–љ–љ—Л–µ –≥–µ–љ—Л —Б–Њ–±—А–∞–љ—Л –≤ –Њ–њ–µ—А–Њ–љ—Л вАФ –≥—А—Г–њ–њ—Л —Б–Њ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л—Е, —Б–Њ—В—А–∞–љ—Б–Ї—А–Є–±–Є—А—Г–µ–Љ—Л—Е –Є —Б–Њ—В—А–∞–љ—Б–ї–Є—А—Г–µ–Љ—Л—Е –≥–µ–љ–Њ–≤. –Я–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Њ–њ–µ—А–Њ–љ–Њ–≤, —Г—З–∞—Б—В–≤—Г—О—Й–Є—Е –≤ –Њ–і–љ–Є—Е –Є —В–µ—Е –ґ–µ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –њ—Г—В—П—Е, —Г —А–∞–Ј–љ—Л—Е –≤–Є–і–Њ–≤ –Љ–Њ–≥—Г—В –њ–µ—А–µ–Ї—А—Л–≤–∞—В—М—Б—П. –Р–≤—В–Њ—А—Л –≤—Л–і–µ–ї–Є–ї–Є –≥–µ–љ—Л, —А–∞—Б–њ–Њ–ї–∞–≥–∞—О—Й–Є–µ—Б—П –≤–±–ї–Є–Ј–Є CRISPR-–ї–Њ–Ї—Г—Б–∞, cas1-–≥–µ–љ–Њ–≤ –Є–ї–Є —Н—Д—Д–µ–Ї—В–Њ—А–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ вАФ –±√≥–ї—М—И–∞—П –Є—Е —З–∞—Б—В—М –±—Л–ї–∞ –Њ–њ–Є—Б–∞–љ–∞ –≤–њ–µ—А–≤—Л–µ. –Ш—Е –љ–∞–Ј–≤–∞–ї–Є CRISPR-—Б–≤—П–Ј–∞–љ–љ—Л–Љ–Є –≥–µ–љ–∞–Љ–Є.
–Т –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ –∞–≤—В–Њ—А—Л –Є–Ј—Г—З–Є–ї–Є –Ї–Њ—Н–≤–Њ–ї—О—Ж–Є—О CRISPR-—Б–≤—П–Ј–∞–љ–љ—Л—Е –≥–µ–љ–Њ–≤ —Б CRISPR-–ї–Њ–Ї—Г—Б–Њ–Љ, –њ–Њ—Б—В—А–Њ–Є–ї–Є —Д–Є–ї–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –і–µ—А–µ–≤—М—П –Є —Б—А–∞–≤–љ–Є–ї–Є –Є—Е —Б –і–µ—А–µ–≤—М—П–Љ–Є cas-–≥–µ–љ–Њ–≤ –Є –і–µ—А–µ–≤—М—П–Љ–Є 16S —А–†–Э–Ъ (–≤ –Ї–∞—З–µ—Б—В–≤–µ –Ї–Њ–љ—В—А–Њ–ї—П). –Ш–љ—В–µ—А–µ—Б–љ–Њ, —З—В–Њ —Н–≤–Њ–ї—О—Ж–Є–Њ–љ–љ—Л–µ —А–∞—Б—Б—В–Њ—П–љ–Є—П –Љ–µ–ґ–і—Г –≥–µ–љ–∞–Љ–Є cas10 (–±–Њ–ї—М—И–Њ–є —Б—Г–±—К–µ–і–Є–љ–Є—Ж—Л —Н—Д—Д–µ–Ї—В–Њ—А–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ —Б–Є—Б—В–µ–Љ II —В–Є–њ–∞) –Є –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ —А–∞—Б—Б—В–Њ—П–љ–Є—П –Љ–µ–ґ–і—Г –≥–µ–љ–∞–Љ–Є corA (–Є–Њ–љ–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞, –Ї–Њ–і–Є—А—Г–µ–Љ–Њ–≥–Њ —Б–Є—Б—В–µ–Љ–∞–Љ–Є –њ–Њ–і—В–Є–њ–∞ III-B) –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г—О—В –Ї–Њ—А—А–µ–ї—П—Ж–Є—О, —З–µ–≥–Њ –љ–µ —Б–Ї–∞–ґ–µ—И—М –њ—А–Њ —Б–≤—П–Ј—М –ї—О–±–Њ–≥–Њ –Є–Ј —Н—В–Є—Е –≥–µ–љ–Њ–≤ —Б 16S –†–Э–Ъ. –Ш–љ—Л–Љ–Є —Б–ї–Њ–≤–∞–Љ–Є, –≥–µ–љ—Л –≤–љ—Г—В—А–Є CRISPR-–°as-–ї–Њ–Ї—Г—Б–∞ –Ї–Њ—Н–≤–Њ–ї—О—Ж–Є–Њ–љ–Є—А—Г—О—В, —В–Њ–≥–і–∞ –Ї–∞–Ї —Б–∞–Љ –ї–Њ–Ї—Г—Б –њ–µ—А–µ–і–∞–µ—В—Б—П –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –≥–Њ—А–Є–Ј–Њ–љ—В–∞–ї—М–љ—Л–Љ –њ–µ—А–µ–љ–Њ—Б–Њ–Љ –≥–µ–љ–Њ–≤ вАФ –Њ–і–љ–Є–Љ –Є–Ј –Ї–ї—О—З–µ–≤—Л—Е –њ—Г—В–µ–є –Љ–Є–Ї—А–Њ–±–љ–Њ–є —Н–≤–Њ–ї—О—Ж–Є–Є [10].
–У–Њ—А–Є–Ј–Њ–љ—В–∞–ї—М–љ—Л–є –њ–µ—А–µ–љ–Њ—Б –≥–µ–љ–Њ–≤ —Е–∞—А–∞–Ї—В–µ—А–µ–љ –љ–µ —В–Њ–ї—М–Ї–Њ –і–ї—П CRISPR-—Б–Є—Б—В–µ–Љ, –љ–Њ –Є –і–ї—П –≥–µ–љ–Њ–≤ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, —Б–ї—Г–ґ–∞—Й–Є—Е –±–∞–Ї—В–µ—А–Є—П–Љ –Њ—А—Г–ґ–Є–µ–Љ –Є —Б—А–µ–і—Б—В–≤–Њ–Љ –Њ–±—Й–µ–љ–Є—П —Б —Б–µ–±–µ –њ–Њ–і–Њ–±–љ—Л–Љ–Є. –Ю–± —Н—В–Њ–Љ —А–∞—Б—Б–Ї–∞–ґ–µ—В —Б–ї–µ–і—Г—О—Й–∞—П –≥–ї–∞–≤–∞.
–Я–Њ–Є—Б–Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤
–Т—В–Њ—А–∞—П –≤–∞–ґ–љ–∞—П —В–µ–Љ–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М—Б–Ї–Њ–є –≥—А—Г–њ–њ—Л –°–µ–≤–µ—А–Є–љ–Њ–≤–∞ вАФ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є, –∞ –Є–Љ–µ–љ–љ–Њ –±–∞–Ї—В–µ—А–Є–Њ—Ж–Є–љ—Л. –≠—В–Њ –≤–µ—Й–µ—Б—В–≤–∞, –≤—Л—А–∞–±–∞—В—Л–≤–∞–µ–Љ—Л–µ –±–∞–Ї—В–µ—А–Є—П–Љ–Є –і–ї—П –±–Њ—А—М–±—Л —Б —Б–µ–±–µ –њ–Њ–і–Њ–±–љ—Л–Љ–Є. –Ъ–∞–Ї –Є —Г –ї—О–±–Њ–≥–Њ –Њ—А—Г–ґ–Є—П, –Љ–Є—И–µ–љ–Є –Є—Е –і–µ–є—Б—В–≤–Є—П –≤ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є –Ї–ї–µ—В–Ї–µ —З—А–µ–Ј–≤—Л—З–∞–є–љ–Њ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л (—А–Є—Б. 3). –Ю—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–љ—Л —Б—А–µ–і–Є –љ–Є—Е –і–ї—П –љ–∞—И–µ–≥–Њ —Б–µ–≥–Њ–і–љ—П—И–љ–µ–≥–Њ —А–∞—Б—Б–Ї–∞–Ј–∞ –Љ–Є–Ї—А–Њ—Ж–Є–љ—Л. –≠—В–Њ –Ї–Њ—А–Њ—В–Ї–Є–µ –њ–µ–њ—В–Є–і—Л, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–Њ–±—А–µ—В–∞—О—В —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ (–љ–∞–њ—А–Є–Љ–µ—А, —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –њ–Њ–і–∞–≤–ї—П—В—М —А–Њ—Б—В –і—А—Г–≥–Є—Е –±–∞–Ї—В–µ—А–Є–є) —В–Њ–ї—М–Ї–Њ –њ–Њ—Б–ї–µ –њ–Њ—Б—В—В—А–∞—Б–ї—П—Ж–Є–Њ–љ–љ–Њ–є –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–Є .
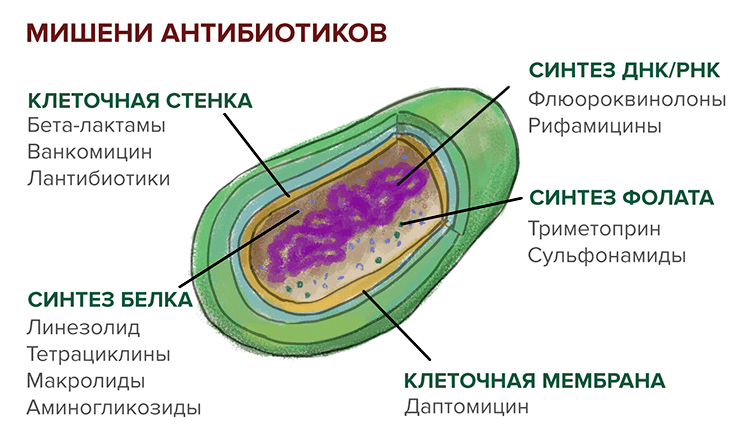
–†–∞–Ј–ї–Є—З–љ—Л–µ –≥—А—Г–њ–њ—Л –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Є –Љ–Є—И–µ–љ–Є –Є—Е –і–µ–є—Б—В–≤–Є—П –≤ –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є –Ї–ї–µ—В–Ї–µ. –Т–Ї—А–∞—В—Ж–µ –Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞—Е –і–µ–є—Б—В–≤–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤: –±–ї–Њ–Ї–Є—А–Њ–≤–∞–љ–Є–µ —Б–Є–љ—В–µ–Ј–∞ –Ї–ї–µ—В–Њ—З–љ–Њ–є —Б—В–µ–љ–Ї–Є –≤–µ–і–µ—В –Ї –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –і–µ–ї–Є—В—М—Б—П –Є —З–∞—Б—В–Њ –Ї –≥–Є–±–µ–ї–Є –±–∞–Ї—В–µ—А–Є–Є; –Њ—Б—В–∞–љ–Њ–≤–Ї–∞ —Б–Є–љ—В–µ–Ј–∞ –±–µ–ї–Ї–∞ –Њ—Б—В–∞–≤–ї—П–µ—В –±–∞–Ї—В–µ—А–Є—О –±–µ–Ј –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л—Е –Љ–∞—И–Є–љ, –≤—Л–њ–Њ–ї–љ—П—О—Й–Є—Е –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤—Б–µ —Д—Г–љ–Ї—Ж–Є–Є; –≤—Б—В—А–∞–Є–≤–∞–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –≤ –Љ–µ–Љ–±—А–∞–љ—Г –≤–ї–µ—З–µ—В –Ј–∞ —Б–Њ–±–Њ–є –љ–∞—А—Г—И–µ–љ–Є–µ –µ–µ –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В–Є –Є –≥–Є–±–µ–ї—М –Њ—В –Њ—Б–Љ–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞; —Д–Њ–ї–∞—В вАФ –Ї–Њ—Д–∞–Ї—В–Њ—А –Љ–љ–Њ–≥–Є—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤, –њ–Њ—Н—В–Њ–Љ—Г –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є–µ –µ–≥–Њ —Б–Є–љ—В–µ–Ј–∞ –Њ—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В —Б–Є–љ—В–µ–Ј –Ф–Э–Ъ/–†–Э–Ъ –Є –±–µ–ї–Ї–Њ–≤; –±–ї–Њ–Ї–Є—А–Њ–≤–∞–љ–Є–µ —Б–Є–љ—В–µ–Ј–∞ –љ—Г–Ї–ї–µ–Є–љ–Њ–≤—Л—Е –Ї–Є—Б–ї–Њ—В –њ—А–Є–≤–Њ–і–Є—В –Ї–∞–Ї –Ї –њ—А–µ–Ї—А–∞—Й–µ–љ–Є—О —Б–Є–љ—В–µ–Ј–∞ –±–µ–ї–Ї–∞, —В–∞–Ї –Є –Ї –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –і–µ–ї–µ–љ–Є—П.
–Т—Б–µ –≤–∞–ґ–љ—Л–µ —Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–Є –Љ–Є–Ї—А–Њ—Ж–Є–љ–Њ–≤ –Ј–∞–Ї–Њ–і–Є—А–Њ–≤–∞–љ—Л –≤ –≥–µ–љ–Њ–Љ–µ –љ–µ—А–∞–Ј—А—Л–≤–љ–Њ —Б ¬Ђ–±–∞–Ј–Њ–≤–Њ–є¬ї –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ–Њ–є –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В—М—О —Б–∞–Љ–Њ–≥–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞: –≤ –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Ф–Э–Ъ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –Ј–∞ –≥√©–љ–Њ–Љ –њ–µ–њ—В–Є–і–∞ —А–∞—Б–њ–Њ–ї–∞–≥–∞—О—В—Б—П –≥–µ–љ—Л —Д–µ—А–Љ–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –µ–≥–Њ –Љ–Њ–і–Є—Д–Є—Ж–Є—А—Г—О—В. –Ґ–∞–Ї–Њ–є –Ї–ї–∞—Б—В–µ—А –ї–µ–≥–Ї–Њ –љ–∞–є—В–Є –≤ –≥–µ–љ–Њ–Љ–µ –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –Љ–µ—В–Њ–і–Њ–≤ –±–Є–Њ–Є–љ—Д–Њ—А–Љ–∞—В–Є–Ї–Є. –Я–Њ –љ–µ–Љ—Г —З–∞—Б—В–Њ –Љ–Њ–ґ–љ–Њ —Б–Ї–∞–Ј–∞—В—М, –Ї–∞–Ї–Њ–є –њ–µ–њ—В–Є–і –њ–Њ–ї—Г—З–Є—В—Б—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г —Д—Г–љ–Ї—Ж–Є–Є –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ —Д–µ—А–Љ–µ–љ—В–Њ–≤-–Љ–Њ–і–Є—Д–Є–Ї–∞—В–Њ—А–Њ–≤ –Є–Ј–≤–µ—Б—В–љ—Л, –Ї–∞–Ї –Є –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В—М –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –њ–µ–њ—В–Є–і–∞.
вАЛ
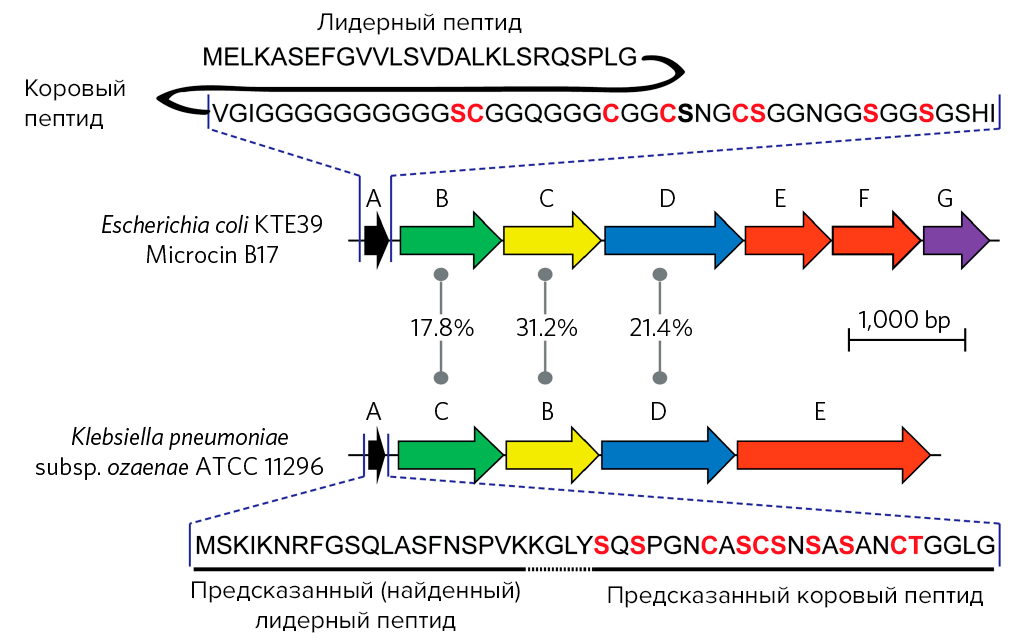
–Т —Б–≤–Њ–µ–є –љ–µ–і–∞–≤–љ–µ–є —Б—В–∞—В—М–µ –≤ Nature Chemical Biology (–Њ–і–љ–Њ–Љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ—А–µ–є—В–Є–љ–≥–Њ–≤—Л—Е –Є —Г–≤–∞–ґ–∞–µ–Љ—Л—Е –Ј–∞—А—Г–±–µ–ґ–љ—Л—Е –ґ—Г—А–љ–∞–ї–Њ–≤) —Б–Њ—В—А—Г–і–љ–Є–Ї–Є –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –Ј–∞–і–∞–ї–Є—Б—М —Ж–µ–ї—М—О –љ–∞–є—В–Є –љ–Њ–≤—Л–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї –Ї–∞–Ї —А–∞–Ј —Б –њ–Њ–Љ–Њ—Й—М—О –±–Є–Њ–Є–љ—Д–Њ—А–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ ¬Ђ–≥–µ–љ–Њ–Љ–љ–Њ–≥–Њ –њ–Њ–Є—Б–Ї–∞¬ї (Genome mining; —Б–Љ. –≤—А–µ–Ј–Ї—Г –љ–Є–ґ–µ –і–ї—П –Њ–±—К—П—Б–љ–µ–љ–Є—П —Н—В–Њ–≥–Њ –∞–ї–≥–Њ—А–Є—В–Љ–∞) [12]. –Т –Ї–∞—З–µ—Б—В–≤–µ ¬Ђ–љ–∞–ґ–Є–≤–Ї–Є¬ї –і–ї—П –њ–Њ–Є—Б–Ї–Њ–≤–Њ–≥–Њ –∞–ї–≥–Њ—А–Є—В–Љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –Є–Ј–≤–µ—Б—В–љ—Л–є —Г E. coli –Љ–Є–Ї—А–Њ—Ж–Є–љ B17 (MccB17) вАФ —Б–Є–ї—М–љ—Л–є –Є–љ–≥–Є–±–Є—В–Њ—А –Ф–Э–Ъ-–≥–Є—А–∞–Ј—Л (–Њ –Ї–Њ—В–Њ—А–Њ–є –љ–Є–ґ–µ —А–µ—З—М –њ–Њ–є–і–µ—В –Њ—В–і–µ–ї—М–љ–Њ), –Ї–Њ–і–Є—А—Г–µ–Љ—Л–є –Ї–ї–∞—Б—В–µ—А–Њ–Љ mcbABCDEFG. –≠—В–Њ—В ¬Ђ–љ–µ–≤–Њ–і¬ї –њ—А–Є–љ–µ—Б –≥–Њ–Љ–Њ–ї–Њ–≥–Є—З–љ—Л–µ –±–µ–ї–Ї–Є –≤ –≥–µ–љ–Њ–Љ–µ –±–∞–Ї—В–µ—А–Є–Є Klebsiella pneumoniae –њ–Њ–і–≤–Є–і–∞ ozaenae, –Њ—А–≥–∞–љ–Є–Ј–Њ–≤–∞–љ–љ—Л–µ –≤ –Њ—З–µ–љ—М –њ–Њ—Е–Њ–ґ–Є–є –Ї–ї–∞—Б—В–µ—А.
Genome mining: –Ї–∞–Ї ¬Ђ–≤—Л—Г–і–Є—В—М¬ї –Є–Ј –Љ–µ—В–∞–≥–µ–љ–Њ–Љ–љ—Л—Е –±–∞–Ј –љ–Њ–≤—Л–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї
–° –њ–Њ–Љ–Њ—Й—М—О –њ–Њ–і—Е–Њ–і–∞ Genome mining (–≥–µ–љ–Њ–Љ–љ—Л–є –њ–Њ–Є—Б–Ї) –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є –њ–Њ–і —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ–Љ –Ъ–Њ–љ—Б—В–∞–љ—В–Є–љ–∞ –°–µ–≤–µ—А–Є–љ–Њ–≤–∞ –Є—Й—Г—В –≤ –Љ–µ—В–∞–≥–µ–љ–Њ–Љ–љ—Л—Е –Њ–±—А–∞–Ј—Ж–∞—Е –±–Є–Њ—Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–µ –Ї–ї–∞—Б—В–µ—А—Л, –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ—Л–µ –Ј–∞ —Б–Є–љ—В–µ–Ј –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤.
–Ь–µ—В–∞–≥–µ–љ–Њ–Љ–љ–Њ–µ —Б–µ–Ї–≤–µ–љ–Є—А–Њ–≤–∞–љ–Є–µ вАФ —Б–µ–Ї–≤–µ–љ–Є—А–Њ–≤–∞–љ–Є–µ –≤—Б–µ–є –Ф–Э–Ъ, —Б–Њ–і–µ—А–ґ–∞—Й–µ–є—Б—П –≤ –њ—А–Њ–±–µ —Б—А–µ–і—Л, –±—Г–і—М —В–Њ –≥—А—Г–љ—В –ї–Є—В–Њ—А–∞–ї–Є, –±–Њ–ї–Њ—В–љ–∞—П –≤–Њ–і–∞ –Є–ї–Є –±–Є–Њ—В–∞ –Ї–Є—И–µ—З–љ–Є–Ї–∞. –°–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –Љ–µ—В–∞–≥–µ–љ–Њ–Љ вАФ —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В—М –≥–µ–љ–Њ–≤ –≤—Б–µ—Е –Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е—Б—П –≤ –њ—А–Њ–±–µ. –Я—А–Є —А–∞–±–Њ—В–µ —Б –љ–Є–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є –љ–µ –Њ–њ—А–µ–і–µ–ї—П—О—В, —З—М—П –Ф–Э–Ъ –Ї–Њ–Љ—Г –њ—А–Є–љ–∞–і–ї–µ–ґ–Є—В; –Њ–љ–Є —Б–µ–Ї–≤–µ–љ–Є—А—Г—О—В –Є –∞–љ–∞–ї–Є–Ј–Є—А—Г—О—В —Б—А–∞–Ј—Г –≤—Б—О —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В—М. –Ю—Б–≤–µ–ґ–Є—В—М –≤ –њ–∞–Љ—П—В–Є –Љ–µ—В–Њ–і—Л —Б–µ–Ї–≤–µ–љ–Є—А–Њ–≤–∞–љ–Є—П –≤—Л –Љ–Њ–ґ–µ—В–µ –њ–Њ —Б—В–∞—В—М–µ ¬Ђ12 –Љ–µ—В–Њ–і–Њ–≤ –≤ –Ї–∞—А—В–Є–љ–Ї–∞—Е: —Б–µ–Ї–≤–µ–љ–Є—А–Њ–≤–∞–љ–Є–µ –љ—Г–Ї–ї–µ–Є–љ–Њ–≤—Л—Е –Ї–Є—Б–ї–Њ—В¬ї [16].
–Ґ–∞–Ї–Њ–є –њ–Њ–Є—Б–Ї —А–∞—Б—Б—З–Є—В–∞–љ –љ–∞ –њ—А–Њ–Ї–∞—А–Є–Њ—В, —В–∞–Ї –Ї–∞–Ї —З–µ—В–Ї–Є–µ –Ї–ї–∞—Б—В–µ—А—Л –≥–µ–љ–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–ґ–љ–Њ –±—Л–ї–Њ –±—Л –Њ–њ—А–µ–і–µ–ї–Є—В—М –±–Є–Њ–Є–љ—Д–Њ—А–Љ–∞—В–Є—З–µ—Б–Ї–Є, —Г —Н—Г–Ї–∞—А–Є–Њ—В –Њ—В—Б—Г—В—Б—В–≤—Г—О—В. –Э–Њ –љ–∞ –±–∞–Ї—В–µ—А–Є—П—Е —В–∞–Ї–Њ–є –њ–Њ–Є—Б–Ї –і–∞–µ—В –њ—А–µ–Ї—А–∞—Б–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л. –Ю–і–љ–Є–Љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –њ–Њ–њ—Г–ї—П—А–љ—Л—Е —Б–њ–Њ—Б–Њ–±–Њ–≤ –≥–µ–љ–Њ–Љ–љ–Њ–≥–Њ –њ–Њ–Є—Б–Ї–∞, –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–є –Є –≤ –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –°–µ–≤–µ—А–Є–љ–Њ–≤–∞, —П–≤–ї—П–µ—В—Б—П –∞–ї–≥–Њ—А–Є—В–Љ antiSMASH [13], –Ї–Њ—В–Њ—А—Л–є –њ—А–Є–Љ–µ–љ—П—О—В –і–ї—П –њ—А–µ–і—Б–Ї–∞–Ј–∞–љ–Є—П –њ—Г—В–µ–є –±–Є–Њ—Б–Є–љ—В–µ–Ј–∞ –≤—В–Њ—А–Є—З–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤. –Т –µ–≥–Њ –Њ—Б–љ–Њ–≤—Г –ї–µ–≥–ї–Њ ¬Ђ–Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є–µ¬ї —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Є—П –≥–µ–љ–Њ–≤ —Б–Є–љ—В–µ–Ј–∞ –і–∞–љ–љ—Л—Е –≤–µ—Й–µ—Б—В–≤ –≤ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Ї–ї–∞—Б—В–µ—А–∞—Е.
|
–Ъ–∞–Ї –≥–µ–љ–Њ–Љ–љ—Л–є –њ–Њ–Є—Б–Ї –њ–Њ–Ј–≤–Њ–ї—П–µ—В –љ–∞—Е–Њ–і–Є—В—М –љ–Њ–≤—Л–µ –Ї–ї–∞—Б—В–µ—А—Л –≥–µ–љ–Њ–≤. –°–≤–µ—А—Е—Г вАФ —Е–Њ—А–Њ—И–Њ –Є–Ј—Г—З–µ–љ–љ—Л–є –Ї–ї–∞—Б—В–µ—А –Є–Ј–≤–µ—Б—В–љ–Њ–≥–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ MccB17 (–Њ–љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –Ї–∞–Ї ¬Ђ–љ–∞–ґ–Є–≤–Ї–∞¬ї –і–ї—П –њ–Њ–Є—Б–Ї–∞). –°–љ–Є–Ј—Г вАФ –љ–∞–є–і–µ–љ–љ—Л–є –≤ –≥–µ–љ–Њ–Љ–µ –Ї–ї–µ–±—Б–Є–µ–ї–ї—Л –Ї–ї–∞—Б—В–µ—А, –Њ—В–≤–µ—З–∞—О—Й–Є–є –Ј–∞ —Б–Є–љ—В–µ–Ј –љ–µ–Є–Ј–≤–µ—Б—В–љ–Њ–≥–Њ –і–Њ —Б–Є—Е –њ–Њ—А –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –Ї–ї–µ–±—Б–∞–Ј–Њ–ї–Є—Ж–Є–љ–∞, –Є–љ–≥–Є–±–Є—В–Њ—А–∞ —В—А–∞–љ—Б–ї—П—Ж–Є–Є. –Ю–±–Њ–Ј–љ–∞—З–µ–љ–Є–µ –≥–µ–љ–Њ–≤ –≤ –Ї–ї–∞—Б—В–µ—А–∞—Е: A вАФ ¬Ђ–Є—Б—Е–Њ–і–љ—Л–є¬ї –≥–µ–љ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–≥–Њ –њ–µ–њ—В–Є–і–∞ (–Љ–Є–Ї—А–Њ—Ж–Є–љ–∞), –њ–Њ–і–ї–µ–ґ–∞—Й–Є–є –њ–Њ—Б—В—В—А–∞–љ—Б–ї—П—Ж–Є–Њ–љ–љ–Њ–є –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–Є; BвАУG вАФ –≥–µ–љ—Л —Д–µ—А–Љ–µ–љ—В–Њ–≤, –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—О—Й–Є—Е —Н—В—Г –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є—О –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П ¬Ђ–Ј—А–µ–ї–Њ–≥–Њ¬ї –њ–µ–њ—В–Є–і–∞. –У–µ–љ—Л —Д–µ—А–Љ–µ–љ—В–Њ–≤ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—П–Љ–Є –Ї–∞–Ї –њ–Њ–Є—Б–Ї–Њ–≤—Л–є –Ј–∞–њ—А–Њ—Б –Ї –Љ–µ—В–∞–≥–µ–љ–Њ–Љ–љ—Л–Љ –і–∞–љ–љ—Л–Љ: –Є–Љ–µ–љ–љ–Њ –њ–Њ –љ–Є–Љ –Є—Й—Г—В –љ–Њ–≤—Л–µ –Ї–ї–∞—Б—В–µ—А—Л, –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –≤ –і–∞–ї—М–љ–µ–є—И–µ–Љ –≤—Л–і–µ–ї—П—О—В –љ–Њ–≤—Л–µ –Љ–Є–Ї—А–Њ—Ж–Є–љ—Л. |
|
|
–Р –Ї–∞–Ї –і–∞–ї—М—И–µ –Є—Й—Г—В –Ї–ї–∞—Б—В–µ—А—Л —Н—В–Є—Е –≥–µ–љ–Њ–≤? –Я–Њ–Є—Б–Ї –њ—А–Њ–≤–Њ–і—П—В –≤ –≥–µ–љ–Њ–Љ–љ—Л—Е –Є–ї–Є –Љ–µ—В–∞–≥–µ–љ–Њ–Љ–љ—Л—Е –і–∞–љ–љ—Л—Е. –Я–Њ—Б–ї–µ —Н—В–Њ–≥–Њ –ї–Є–±–Њ –±–µ—А—Г—В —И—В–∞–Љ–Љ –±–∞–Ї—В–µ—А–Є–Є, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –±—Л–ї –љ–∞–є–і–µ–љ –Ї–ї–∞—Б—В–µ—А, –Є –≤—Л–і–µ–ї—П—О—В –Є–Ј –љ–µ–≥–Њ –Є–Ј—Г—З–∞–µ–Љ—Л–є –±–µ–ї–Њ–Ї, –ї–Є–±–Њ —Н–Ї—Б–њ—А–µ—Б—Б–Є—А—Г—О—В –µ–≥–Њ –≤ –і—А—Г–≥–Њ–Љ —И—В–∞–Љ–Љ–µ-–њ—А–Њ–і—Г—Ж–µ–љ—В–µ. –Ш –љ–∞–Ї–Њ–љ–µ—Ж –Љ–Њ–ґ–љ–Њ –њ—А–Є—Б—В—Г–њ–∞—В—М –Ї –Є–Ј—Г—З–µ–љ–Є—О –µ–≥–Њ —Б–≤–Њ–є—Б—В–≤, –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –і–µ–є—Б—В–≤–Є—П –Є –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л—Е –Љ–Є—И–µ–љ–µ–є. –°—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–є –љ–µ–і–Њ—Б—В–∞—В–Њ–Ї –Љ–µ—В–Њ–і–∞ –≤ —В–Њ–Љ, —З—В–Њ –Њ–љ –Њ—Б–љ–Њ–≤–∞–љ –љ–∞ –≥–Њ–Љ–Њ–ї–Њ–≥–Є–Є –≥–µ–љ–Њ–≤ –±–µ–ї–Ї–Њ–≤, –Љ–Њ–і–Є—Д–Є—Ж–Є—А—Г—О—Й–Є—Е –Љ–Є–Ї—А–Њ—Ж–Є–љ, —Б –Є–Ј–≤–µ—Б—В–љ—Л–Љ–Є –≥–µ–љ–∞–Љ–Є. –Э–∞–є—В–Є –љ–µ–≥–Њ–Љ–Њ–ї–Њ–≥–Є—З–љ—Л–µ –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В–Є —В–∞–Ї–Є–Љ —Б–њ–Њ—Б–Њ–±–Њ–Љ –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ. |
|
|
–Я–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В—М –њ—А–µ–і—И–µ—Б—В–≤–µ–љ–љ–Є–Ї–∞ –њ—А–µ–і—Б–Ї–∞–Ј–∞–љ–љ–Њ–≥–Њ –Љ–Є–Ї—А–Њ—Ж–Є–љ–∞ KlpA –љ–µ –±—Л–ї–∞ –њ–Њ—Е–Њ–ґ–∞ –љ–∞ –Є–Ј–≤–µ—Б—В–љ—Л–µ —А–∞–љ–µ–µ –Љ–Є–Ї—А–Њ—Ж–Є–љ—Л, –∞ –Ј–љ–∞—З–Є—В, –Ј—А–µ–ї—Л–є KlpA –і–Њ–ї–ґ–µ–љ –±—Л–ї –Є–Љ–µ—В—М –љ–µ–Њ–±—Л—З–љ—Г—О —Б—В—А—Г–Ї—В—Г—А—Г –Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є. –Э–∞–є–і–µ–љ–љ—Л–є –Љ–Є–Ї—А–Њ—Ж–Є–љ —А–µ—И–Є–ї–Є –љ–∞–Ј–≤–∞—В—М –Ї–ї–µ–±—Б–∞–Ј–Њ–ї–Є—Ж–Є–љ–Њ–Љ (KLB, —А–Є—Б. 5) вАФ –њ–Њ —А–Њ–і—Г –±–∞–Ї—В–µ—А–Є–Є, –≤ –Ї–Њ—В–Њ—А–Њ–є –Њ–љ —Б–Є–љ—В–µ–Ј–Є—А—Г–µ—В—Б—П. –Ґ–∞–Ї –±—Л–ї –љ–∞–є–і–µ–љ –љ–Њ–≤—Л–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї. –Э–Њ —Б–∞–Љ–Њ–µ –Є–љ—В–µ—А–µ—Б–љ–Њ–µ вАФ –Љ–µ—Е–∞–љ–Є–Ј–Љ –µ–≥–Њ –і–µ–є—Б—В–≤–Є—П. –І—В–Њ–±—Л —Г–і–Њ—Б—В–Њ–≤–µ—А–Є—В—М—Б—П, —П–≤–ї—П–µ—В—Б—П –ї–Є –Ї–ї–µ–±—Б–∞–Ј–Њ–ї–Є—Ж–Є–љ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Љ —В—А–∞–љ—Б–ї—П—Ж–Є–Є, –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є in vitro —Б–Є—Б—В–µ–Љ—Г —Б–Є–љ—В–µ–Ј–∞ –ї—О—Ж–Є—Д–µ—А–∞–Ј—Л. –≠—В–∞ —Б–Є—Б—В–µ–Љ–∞ –њ–Њ–і—А–∞–Ј—Г–Љ–µ–≤–∞–µ—В –љ–∞–ї–Є—З–Є–µ –≤ –њ—А–Њ–±–Є—А–Ї–µ –≤—Б–µ—Е —А–µ–∞–≥–µ–љ—В–Њ–≤ —А–µ–∞–Ї—Ж–Є–Є –Њ–Ї–Є—Б–ї–µ–љ–Є—П –ї—О—Ж–Є—Д–µ—А–Є–љ–∞, –Ї—А–Њ–Љ–µ –ї—О—Ж–Є—Д–µ—А–∞–Ј—Л (—В–Њ –µ—Б—В—М —Б–∞–Љ –ї—О—Ж–Є—Д–µ—А–Є–љ, –Р–Ґ–§ –Є –Ї–Є—Б–ї–Њ—А–Њ–і), –∞ —В–∞–Ї–ґ–µ —А–Є–±–Њ—Б–Њ–Љ –Є –Љ–†–Э–Ъ –≥–µ–љ–∞ –ї—О—Ж–Є—Д–µ—А–∞–Ј—Л. –Т –і–∞–љ–љ–Њ–Љ —Б–ї—Г—З–∞–µ –≤ –њ—А–Њ–±–Є—А–Ї—Г —В–∞–Ї–ґ–µ –і–Њ–±–∞–≤–ї—П–ї–Є –Є–љ–≥–Є–±–Є—В–Њ—А —В—А–∞–љ—Б–ї—П—Ж–Є–Є. –Ъ–Њ–≥–і–∞ –Є–љ–≥–Є–±–Є—В–Њ—А —А–∞–±–Њ—В–∞–µ—В, —В—А–∞–љ—Б–ї—П—Ж–Є—П –њ–Њ–і–∞–≤–ї—П–µ—В—Б—П, –Є —Б–≤–µ—З–µ–љ–Є–µ –њ—А–Њ–њ–∞–і–∞–µ—В. –Ґ–∞–Ї –Є —Б–ї—Г—З–Є–ї–Њ—Б—М –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –Ї–ї–µ–±—Б–∞–Ј–Њ–ї–Є—Ж–Є–љ–∞, –∞ –Ј–љ–∞—З–Є—В, –Њ–љ –±–ї–Њ–Ї–Є—А—Г–µ—В –Є–Љ–µ–љ–љ–Њ —А–∞–±–Њ—В—Г —А–Є–±–Њ—Б–Њ–Љ—Л. –І—В–Њ–±—Л —А–∞–Ј–Њ–±—А–∞—В—М—Б—П –≤ –Љ–µ—Е–∞–љ–Є–Ј–Љ–µ —Н—В–Њ–≥–Њ –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є—П, –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є –Є–Ј –°–Ї–Њ–ї—В–µ—Е–∞ –Њ–±—К–µ–і–Є–љ–Є–ї–Є —Г—Б–Є–ї–Є—П —Б –Ї–Њ–ї–ї–µ–≥–∞–Љ–Є –Є–Ј –І–Є–Ї–∞–≥–Њ, —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А—Г—О—Й–Є–Љ–Є—Б—П –љ–∞ —Б—В—А—Г–Ї—В—Г—А–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —А–Є–±–Њ—Б–Њ–Љ—Л. –У—А—Г–њ–њ–∞ –њ–Њ–і —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ–Љ –Ѓ.–°. –Я–Њ–ї–Є–Ї–∞–љ–Њ–≤–∞ –Є–Ј –£–љ–Є–≤–µ—А—Б–Є—В–µ—В–∞ –Ш–ї–ї–Є–љ–Њ–є—Б–∞ –Ј–∞–Ї—А–Є—Б—В–∞–ї–ї–Є–Ј–Њ–≤–∞–ї–∞ —А–Є–±–Њ—Б–Њ–Љ—Л Thermus thermophilus –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є KLB, –Љ–†–Э–Ъ –Є —В–†–Э–Ъ –≤ –Р-, –†- –Є –Х-—Б–∞–є—В–∞—Е –Є —Г—Б—В–∞–љ–Њ–≤–Є–ї–∞ 3D-—Б—В—А—Г–Ї—В—Г—А—Г –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ —Б —А–∞–Ј—А–µ—И–µ–љ–Є–µ–Љ 2,7 √Е, –Њ–њ–Є—А–∞—П—Б—М –љ–∞ —Г–ґ–µ –Є–Ј–≤–µ—Б—В–љ—Г—О –Љ–Њ–і–µ–ї—М —А–Є–±–Њ—Б–Њ–Љ—Л —Н—В–Њ–є –±–∞–Ї—В–µ—А–Є–Є. –Ю–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ –Ї–ї–µ–±—Б–∞–Ј–Њ–ї–Є—Ж–Є–љ –Ј–∞–Ї—А—Л–≤–∞–µ—В —В—Г–љ–љ–µ–ї—М –≤—Л—Е–Њ–і–∞ —А–∞—Б—В—Г—Й–µ–≥–Њ –њ–µ–њ—В–Є–і–∞ –≤ –±–Њ–ї—М—И–Њ–є —Б—Г–±—К–µ–і–Є–љ–Є—Ж–µ (—А–Є—Б. 5). –Т —Б—В–∞—В—М–µ –∞–≤—В–Њ—А—Л —В–∞–Ї–ґ–µ —Б—А–∞–≤–љ–Є–ї–Є —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ –Ї–ї–µ–±—Б–∞–Ј–Њ–ї–Є—Ж–Є–љ–∞ —Б –і—А—Г–≥–Є–Љ–Є —А–Є–±–Њ—Б–Њ–Љ–љ—Л–Љ–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є, –∞ –Є–Љ–µ–љ–љ–Њ —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ–Њ–Љ –Є —Е–Є–љ—Г–њ—А–Є—Б—В–Є–љ–Њ–Љ.
–Т —А–∞–±–Њ—В–µ —Г—З–∞—Б—В–≤–Њ–≤–∞–ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М—Б–Ї–Є–µ –≥—А—Г–њ–њ—Л —А–∞–Ј–љ—Л—Е –≤—Г–Ј–Њ–≤ –Є –Є–љ—Б—В–Є—В—Г—В–Њ–≤: –Я–Њ–ї–Є—В–µ—Е–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В–∞ –Є –Ш–љ—Б—В–Є—В—Г—В–∞ —П–і–µ—А–љ–Њ–є —Д–Є–Ј–Є–Ї–Є (–°–∞–љ–Ї—В-–Я–µ—В–µ—А–±—Г—А–≥), –Ш–љ—Б—В–Є—В—Г—В–∞ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є —Е–Є–Љ–Є–Њ—В–µ—А–∞–њ–Є–Є (–°–Љ–Њ–ї–µ–љ—Б–Ї), –°–Ї–Њ–ї—В–µ—Е–∞, –Ш–љ—Б—В–Є—В—Г—В–∞ –±–Є–Њ–ї–Њ–≥–Є–Є –≥–µ–љ–∞ –†–Р–Э, –Ь–У–£ (—Д–∞–Ї—Г–ї—М—В–µ—В–Њ–≤: —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ, –±–Є–Њ–Є–љ–ґ–µ–љ–µ—А–Є–Є –Є –±–Є–Њ–Є–љ—Д–Њ—А–Љ–∞—В–Є–Ї–Є, –∞ —В–∞–Ї–ґ–µ –Ш–љ—Б—В–Є—В—Г—В–∞ –С–µ–ї–Њ–Ј–µ—А—Б–Ї–Њ–≥–Њ) (–Ь–Њ—Б–Ї–≤–∞), –£–љ–Є–≤–µ—А—Б–Є—В–µ—В–∞ –Ш–ї–ї–Є–љ–Њ–є—Б–∞ –Є –Ш–љ—Б—В–Є—В—Г—В–∞ –Т–∞–Ї—Б–Љ–∞–љ–∞ (–°–®–Р).
|
–І–Є—В–∞—В—М –њ–Њ–і—А–Њ–±–љ–µ–µ: –С–Є–Њ–Љ–Њ–ї–µ–Ї—Г–ї–∞




